パーキンソン病とは?
パーキンソン病は、脳内で運動を調節する神経細胞が徐々に失われていく進行性の神経疾患です。特に「ドーパミン」という神経伝達物質を作り出す細胞が減っていくことで、以下のような症状が現れます。
- 手足の震え(振戦)
- 筋肉のこわばり(固縮)
- 動作が遅くなる(寡動・無動)
- 歩行時のバランス障害
これらの運動症状に加えて、抑うつ、便秘、睡眠障害、嗅覚低下などの非運動症状も多く、患者さんの生活の質(QOL)を大きく低下させる病気です。
現在の治療とその限界
現在広く行われている治療は、薬物療法(ドーパミン補充薬やアゴニスト)や脳深部刺激術(DBS)などです。これらは症状を一時的に和らげることはできますが、病気の進行を止めたり根本的に治すことはできません。
そのため、従来の治療に加えて「病気そのものにアプローチする治療」が必要とされており、そこで注目されているのが幹細胞治療です。
幹細胞治療への期待
幹細胞とは、さまざまな細胞に分化し、体の修復や再生を促す特殊な細胞です。パーキンソン病に対する細胞治療の研究は1980年代から始まっており、当時は胎児の脳組織移植も試みられました。しかし、倫理的な問題や技術的な課題があり実用化には至りませんでした。
近年では技術の進歩により、患者さん自身やドナー由来の幹細胞を培養して利用する方法が現実的なものとなっています。特に、自分の脂肪組織から取り出せる幹細胞は入手が容易で拒絶反応のリスクも低く、安全性の面からも新しい治療の可能性として期待されています。

幹細胞治療が期待される理由
幹細胞治療がパーキンソン病の新しい選択肢として注目されているのは、大きく分けて2つの理由があります。
1つは神経の再生・補充です。幹細胞には神経細胞に分化する力があり、失われたドーパミン神経を補う可能性があります。もう1つは脳環境の改善で、幹細胞そのものが分化しなくても、神経を守ったり修復を助けるさまざまな物質を分泌してくれるのです。
具体的には、幹細胞は脳内で神経の成長を促す栄養因子(神経栄養因子)や細胞の生存を支える物質を放出します。さらに、パーキンソン病で問題となる脳内の炎症や免疫の乱れを和らげ、慢性的な炎症を抑える抗炎症サイトカインも分泌します。
つまり幹細胞は「神経を生み出し、守り、育てる」多面的な作用を持ち、病気の進行を遅らせたり症状を改善したりする可能性があるのです。
実際に動物実験では、パーキンソン病モデルのマウスに幹細胞を移植すると運動機能が改善し、脳内で減少していたドーパミン産生神経が回復した例が繰り返し報告されています。これらの結果は、幹細胞が新しい神経細胞を生み出すだけでなく、残っている神経を保護していることを示唆しています。
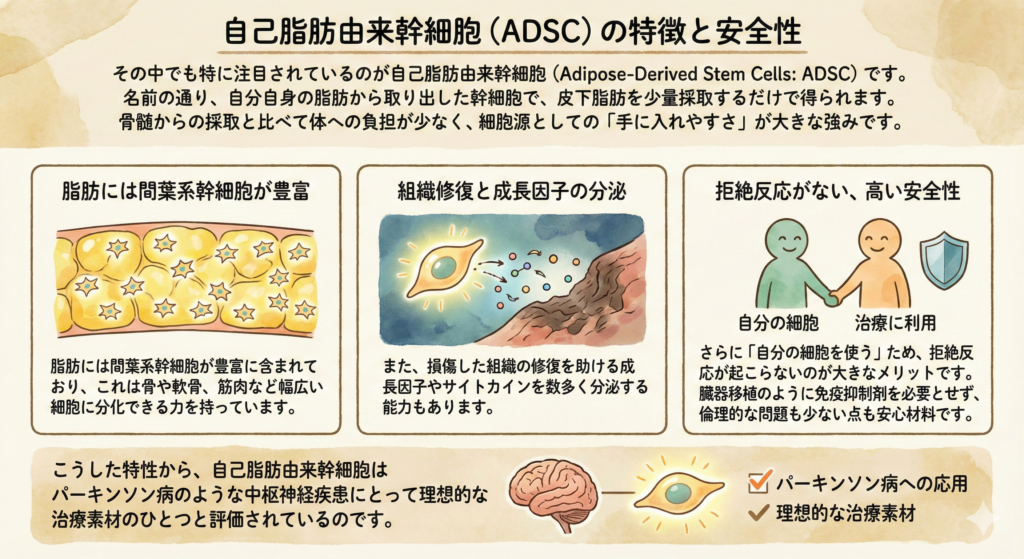
自己脂肪由来幹細胞(ADSC)の特徴と安全性
その中でも特に注目されているのが自己脂肪由来幹細胞(Adipose-Derived Stem Cells: ADSC)です。名前の通り、自分自身の脂肪から取り出した幹細胞で、皮下脂肪を少量採取するだけで得られます。骨髄からの採取と比べて体への負担が少なく、細胞源としての「手に入れやすさ」が大きな強みです。
脂肪には間葉系幹細胞が豊富に含まれており、これは骨や軟骨、筋肉など幅広い細胞に分化できる力を持っています。また、損傷した組織の修復を助ける成長因子やサイトカインを数多く分泌する能力もあります。
さらに「自分の細胞を使う」ため、拒絶反応が起こらないのが大きなメリットです。臓器移植のように免疫抑制剤を必要とせず、倫理的な問題も少ない点も安心材料です。胚性幹細胞(受精卵由来)に比べて腫瘍形成リスクも極めて低いとされ、多くの研究で高い安全性が確認されています。
こうした特性から、自己脂肪由来幹細胞はパーキンソン病のような中枢神経疾患にとって理想的な治療素材のひとつと評価されているのです。
点滴・髄腔内投与による治療の方法と流れ
自己脂肪由来幹細胞を使った治療は、
① 患者さんから幹細胞を採取・培養する工程
② その幹細胞を体に戻す工程
の2段階で行われます。
まず腹部などから少量の脂肪を採取します。これは局所麻酔で行う小規模な脂肪吸引のような処置で、多くは日帰りまたは短期入院で済みます。採取した脂肪から幹細胞を分離し、国の認可を受けた培養施設で必要な数まで増やします。
用意された幹細胞は、次の2つの方法で体内に戻します。
静脈点滴:腕の静脈から点滴で投与。1〜2時間かけて行い、投与中は血圧や脈拍を監視します。幹細胞は全身を巡り、分泌される有効成分が血液を介して脳に届くと考えられています。
髄腔内投与:腰から針を刺して脊髄を包む髄液の中に幹細胞を注入。処置時間は1時間程度で、より直接的に中枢神経へ届く可能性があります。ただし腰椎穿刺に伴い頭痛など軽い副作用のリスクがあります。
いずれも処置後は安静と経過観察を行い、問題がなければ帰宅可能です。現在の研究では一定の間隔で複数回投与することで効果が続くかを検証しており、日本の小規模研究では数回の点滴を繰り返しても副作用はなく、安全に実施できたと報告されています。
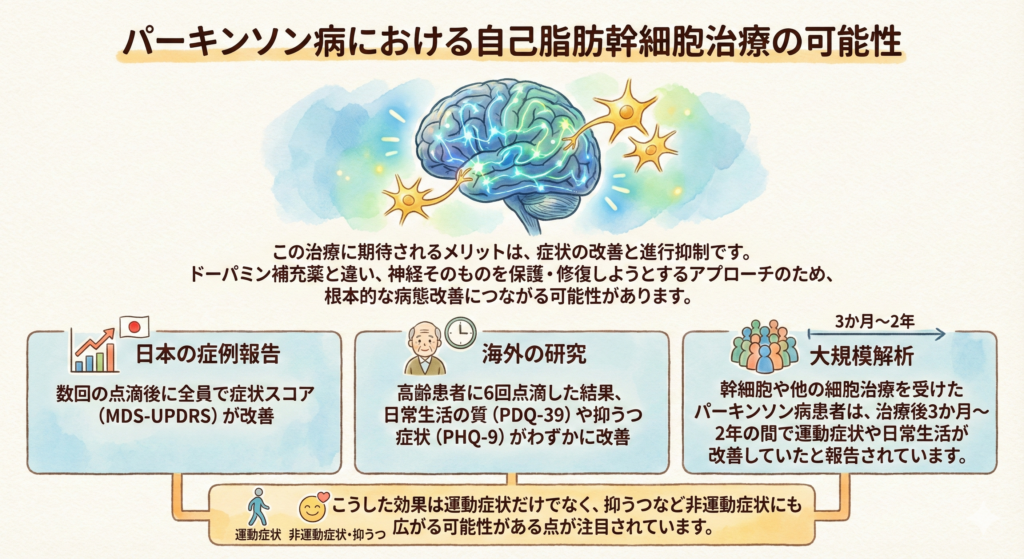
パーキンソン病における自己脂肪幹細胞治療の可能性
この治療に期待されるメリットは、症状の改善と進行抑制です。ドーパミン補充薬と違い、神経そのものを保護・修復しようとするアプローチのため、根本的な病態改善につながる可能性があります。
- 日本の症例報告では、数回の点滴後に全員で症状スコア(MDS-UPDRS)が改善
- 海外の研究では、高齢患者に6回点滴した結果、日常生活の質(PDQ-39)や抑うつ症状(PHQ-9)がわずかに改善
大規模解析でも、幹細胞や他の細胞治療を受けたパーキンソン病患者は、治療後3か月〜2年の間で運動症状や日常生活が改善していたと報告されています。こうした効果は運動症状だけでなく、抑うつなど非運動症状にも広がる可能性がある点が注目されています。
限界と課題
一方で、この治療にはまだ限界もあります。
- 研究段階であり、効果の大きさや持続期間は人によって異なる。
- 改善は「劇的に症状が消える」よりも「多少良くなる」という程度のケースが多い。
- 現時点では統計的に明確な有効性は示されておらず、プラセボ比較など厳密な検証が必要。
つまり、自己脂肪幹細胞治療はパーキンソン病の新しい光ではあるものの、まだ「標準治療」には至っていません。
最新の臨床研究・症例報告から読み解く現状
自己脂肪由来幹細胞を使ったパーキンソン病治療は、まだ研究段階ではありますが、国内外で少しずつ臨床データが蓄積されてきています。
アメリカの研究では、平均80歳と高齢の患者10名に対し、幹細胞を6回静脈点滴する試験が行われました。その結果、重い副作用はなく安全に施行でき、運動機能や生活の質に関する指標でわずかながら改善傾向が確認されました。研究チームは「高齢者においても安全に投与できることが示され、症状改善の可能性がある」と結論づけ、今後は大規模な比較試験で有効性を検証すべきと述べています。
さらに症例報告では、2年間に26回もの点滴を繰り返した患者で、パーキンソン病の症状評価(UPDRSスコア)が明らかに改善し、日常生活動作も向上した例が報告されています。この患者さんでは長期投与中も大きな副作用はなく、PET検査でも脳の代謝が改善していたことが確認され、幹細胞治療が実際に脳内機能を支えた可能性が示唆されました。
一方で、厳密なプラセボ対照試験はまだ限られています。アメリカでは24名規模の第II相試験が2023年に完了しており、安全性と効果をプラセボ群と比較検証中です。今後、このような質の高い研究から得られるデータによって、幹細胞治療の有効性についてより確かな判断ができるようになるでしょう。
現在までの研究を総合すると、「安全性はおおむね良好」「症状に改善を示す例がある」という点では一致しているといえます。
治療を受ける際の注意点と今後の展望
自己脂肪由来幹細胞治療は一部の研究機関やクリニックで先進医療・臨床研究として提供されていますが、受ける際にはいくつかの注意点があります。
まず、十分な説明を受け、納得した上で治療を選ぶことが大切です。効果には個人差があり、現時点では「必ず効く治療」ではありません。標準治療をやめてまで選ぶものではなく、あくまで補助的な位置づけとして慎重に判断する必要があります。
また、この治療は保険適用外である場合が多く、費用が高額になりやすい点も考慮が必要です。加えて、脂肪採取時の内出血や感染、点滴中のアレルギー反応、髄腔内投与での頭痛など、一定の副作用リスクもゼロではありません。必ず信頼できる医療機関で説明を受け、メリットとリスクを理解したうえで治療に臨むことが大切です。
今後の展望
自己脂肪由来幹細胞治療は、パーキンソン病の新しい治療オプションとして大きな期待を集めています。今後の臨床試験の結果次第では、標準治療の一つとして導入される可能性もあります。
さらに将来的には、幹細胞治療とリハビリ、薬物療法を組み合わせた「統合的な治療戦略」も検討されるでしょう。幹細胞で脳内環境を整えつつ、薬やリハビリで補強することで相乗効果が期待されます。
パーキンソン病に苦しむ患者さんにとって、幹細胞治療はまだ道半ばの研究段階ではありますが、確かな希望の光となりつつあります。

よくある質問(FAQ)
自己脂肪幹細胞治療でパーキンソン病の症状がどの程度改善しますか?
症状の改善には個人差がありますが、運動機能の向上や日常生活動作の改善、非運動症状(抑うつ・睡眠障害など)の軽減が報告されています。ただし、完全な治癒ではなく、症状の進行を遅らせたり軽減したりすることが目的です。
幹細胞治療は安全ですか?副作用はありますか?
これまでの研究では重大な副作用は報告されておらず、概ね安全と考えられています。ただし、脂肪採取時の内出血や感染、投与後の軽度な頭痛・倦怠感などが一時的に見られることがあります。
幹細胞治療を受ける際の痛みや負担は大きいですか?
脂肪採取は局所麻酔で行われ、比較的負担は軽い処置です。点滴投与は通常の点滴と同程度、髄腔内投与(腰椎穿刺)は少々の違和感や痛みを伴うことがありますが、一般的に耐えられる範囲内です。
一度治療を受ければ効果はずっと続きますか?
治療の効果持続期間はまだ研究中ですが、多くの臨床研究では複数回の治療で効果が高まると報告されています。一度の治療では数ヶ月から1年程度の効果が期待されるものの、効果を維持するには定期的な投与が必要になる可能性があります。
幹細胞治療は他の治療法(薬物治療、リハビリ)と併用可能ですか?
はい、幹細胞治療は通常の薬物治療やリハビリと併用可能です。むしろ併用することで相乗効果が期待されますので、標準的な治療は継続しつつ幹細胞治療を取り入れる形になります。
治療を受けられないケースはありますか?
重篤な感染症、がん治療中、免疫疾患をお持ちの方、妊娠中の方は治療を控える場合があります。治療前には必ず医師の詳しい診断と評価が必要です。
幹細胞治療は保険が適用されますか?
現在、この治療法は研究段階であり自由診療のため、保険は適用されません。費用が高額になることもありますので、事前に医療機関に確認してください。
治療後の日常生活で特に注意すべきことはありますか?
治療直後は疲れや倦怠感が出ることもありますので、数日間はゆったりと過ごすことをお勧めします。その後は通常の生活に戻れますが、主治医の指示に従い定期的な経過観察を行いましょう。
自己脂肪幹細胞治療の将来性について、現段階ではどう評価されていますか?
現在は研究段階ですが、安全性が高く初期の有効性も報告されているため、将来的にはパーキンソン病の新たな治療法として有望とされています。ただし、明確なエビデンス確立にはさらなる臨床試験が必要です。
治療を受けるにはどのような施設を選ぶべきでしょうか?
国の認定を受けた再生医療施設や研究実績のある専門機関で、十分な説明やフォローアップ体制が整っている施設を選びましょう。まずは主治医とよく相談し、信頼できる機関での治療を検討してください。
まとめ
自己脂肪由来幹細胞を用いたパーキンソン病治療は「自分の細胞で自分の脳を守る」という夢のあるアプローチであり、現在その安全性は概ね確認されつつあります。効果についても初期ながら有望な結果が報告されており、今後の大規模試験で有効性が証明されれば新たな治療の柱になるかもしれません。一方で、まだ研究段階であることを忘れず、最新の情報に基づいて慎重に判断することが大切です。主治医ともよく相談し、信頼できる体制のもとで治療を受けるようにしましょう。研究者たちは「希望は十分にある」としながらも、更なる検証と改良を重ねてこの治療を洗練させようと取り組んでいます。患者さん・ご家族にとっても希望を持ちつつ現実的な視点を失わず、正しい情報に基づいて治療と向き合っていただければと思います。
引用文献(バンクーバースタイル)
1. Fričová D, Korchak JA, Zubair AC. Challenges and translational considerations of mesenchymal stem/stromal cell therapy for Parkinson’s disease. NPJ Regenerative Medicine. 2020;5(1):20.
2. Li K, Li X, Shi G, et al. Effectiveness and mechanisms of adipose-derived stem cell therapy in animal models of Parkinson’s disease: a systematic review and meta-analysis. Translational Neurodegeneration. 2021;10(1):14.
3. Wang F, Sun Z, Peng D, et al. Cell-therapy for Parkinson’s disease: a systematic review and meta-analysis. Journal of Translational Medicine. 2023;21(1):601.
4. Wu H, Fan Y, Zhang M. Advanced progress in the role of adipose-derived mesenchymal stromal/stem cells in the application of central nervous system disorders. Pharmaceutics. 2023;15(11):2637.
5. Schiess M, Suescun J, Doursout MF, et al. Allogeneic bone marrow–derived mesenchymal stem cell safety in idiopathic Parkinson’s disease. Movement Disorders. 2021;36(8):1825-1834.
6. Shigematsu K, Komori N, Tahara K, Yamagishi H. Repeated infusion of autologous adipose tissue-derived stem cells for Parkinson’s disease. Acta Neurologica Scandinavica. 2022;145(1):119-122.
7. Vij R, Prossin A, Tripathy M, et al. Long-term, repeated doses of intravenous autologous mesenchymal stem cells for a patient with Parkinson’s disease: a case report. Frontiers in Neurology. 2023;14:1257080.
8. Vij R, Kim H, Park H, et al. Safety and efficacy of adipose-derived mesenchymal stem cell therapy in elderly Parkinson’s disease patients: an intermediate-size expanded access program. Cytotherapy. 2025;27(2):181-187.
9. International Parkinson and Movement Disorder Society (MDS) Scientific Issues Committee. MDS Position Paper – Use of Stem Cell Therapies for Parkinson’s Disease. January 2021.
最終更新日:2026.03.05





とは?老化を招く体内の焦げつき-150x84.png)






