アムシェプリは、住友ファーマが開発した世界初のiPS細胞由来再生医療等製品で、2026年5月に薬価5,530万円で保険適用が決まったパーキンソン病の新しい治療選択肢です。レボドパで効果が不十分な患者さんを対象に、iPS細胞からつくったドパミン神経前駆細胞を定位脳手術で被殻に移植する細胞治療で、条件・期限付承認のもと、今後7年間でエビデンスが本格的に積み上げられます。本記事では、再生医療専門医がアムシェプリの治療法・薬価・保険適用条件・京大Phase I/II試験の最新エビデンス、そして自家脂肪由来幹細胞(ADSC)治療との違いまで一気通貫で解説します。
- アムシェプリとは?パーキンソン病に対する世界初のiPS細胞治療を医師が解説
- なぜパーキンソン病に「新しい治療薬」が必要だったのか
- アムシェプリの治療法——定位脳手術と被殻への細胞移植
- 薬価5,530万円とパーキンソン病における保険適用——患者負担はどうなるか
- 京大Phase I/II試験のエビデンス——パーキンソン病iPS細胞治療で何が示されたか
- もう一つの選択肢——自家脂肪由来幹細胞(ADSC)治療
- アムシェプリ vs 自家脂肪由来幹細胞(ADSC)治療——どう選ぶか
- パーキンソン病でお悩みの方へ——Cell Grand Clinicができるサポート
- FAQ——よくある質問
- まとめ——希望と現実、両方を持って前に進む
- 関連コラム
- 引用文献
アムシェプリとは?パーキンソン病に対する世界初のiPS細胞治療を医師が解説
▼ ダイレクトアンサー アムシェプリは、他家iPS細胞からドパミン神経前駆細胞を作製した再生医療等製品で、レボドパで十分な効果が得られないパーキンソン病患者さんに対し、定位脳手術により脳内(被殻)へ細胞を移植する治療です。住友ファーマが開発し、2026年3月に条件・期限付承認、5月20日から保険適用が開始されました。
アムシェプリ(一般名:ドパミン神経前駆細胞)は、京都大学iPS細胞研究所(CiRA)で長年積み上げられてきた基礎・臨床研究を基盤として、住友ファーマが製造販売承認を取得した世界初のiPS細胞由来再生医療等製品です。
パーキンソン病は、脳の中で運動を制御するドパミンを産生する神経細胞が減少していくことで、振戦・筋強剛・無動・姿勢反射障害などの運動症状が進行する神経変性疾患です。レボドパなどの薬物療法で症状はコントロールできますが、進行に伴い「ウェアリングオフ」「ジスキネジア」が起こり、薬物療法だけでは生活の質を保ちにくくなります。アムシェプリは「足りなくなった細胞そのものを補う」という、薬物療法とは根本的に異なる治療コンセプトです。
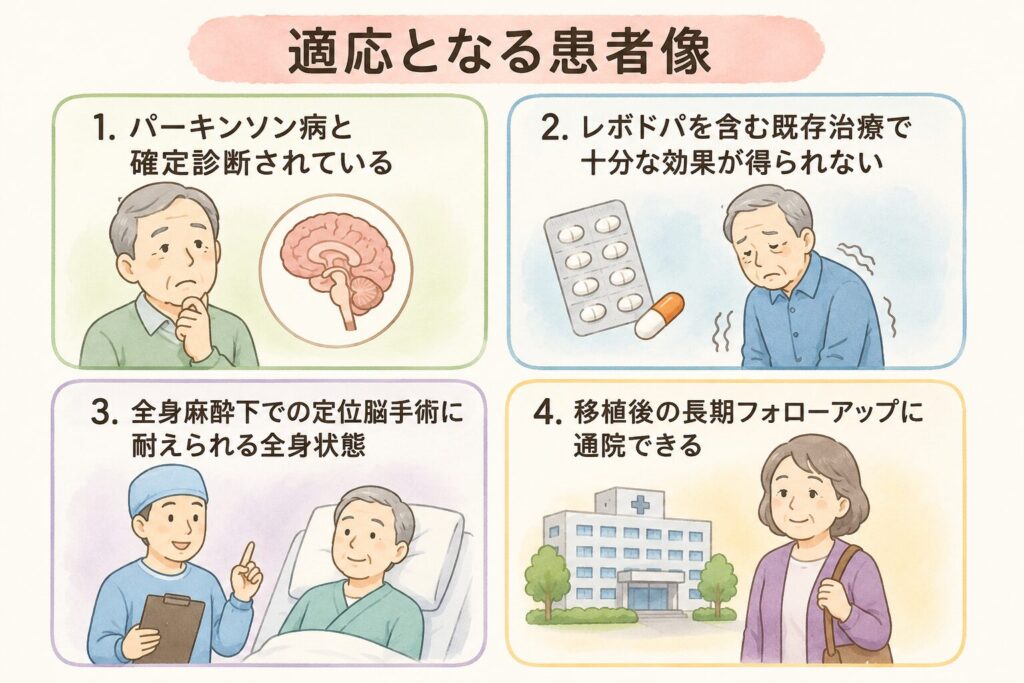
適応となる患者像
- パーキンソン病と確定診断されている
- レボドパを含む既存治療で十分な効果が得られない
- 全身麻酔下での定位脳手術に耐えられる全身状態
- 移植後の長期フォローアップに通院できる
なぜパーキンソン病に「新しい治療薬」が必要だったのか
▼ ダイレクトアンサー パーキンソン病は薬物療法(レボドパ)や脳深部刺激療法(DBS)で症状を抑えられますが、病気の進行そのものを止める治療はこれまで存在しませんでした。進行期には薬の効果が短くなるウェアリングオフ、不随意運動のジスキネジアが起こり、新薬と新しい治療コンセプトが長年待たれてきました。
国内のパーキンソン病患者数は推計で約20万人とされ、高齢化に伴い増加傾向にあります。標準治療は1960年代に登場したレボドパ補充療法を中心に、ドパミンアゴニスト、MAO-B阻害薬、COMT阻害薬などが追加されてきました。これらは症状を抑える対症療法であり、減少していく神経細胞を補ったり、進行を止めたりする力はありません。
DBS(脳深部刺激療法)は1990年代以降に普及した手術療法で、振戦やジスキネジアの軽減に有効ですが、これも神経そのものを再生するわけではありません。
このような背景から、長年「病気の進行に直接アプローチできる治療」が求められてきました。アムシェプリはまさにこの「ミッシングピース」を埋めようとする治療です。
アムシェプリの治療法——定位脳手術と被殻への細胞移植
▼ ダイレクトアンサー アムシェプリの投与は、全身麻酔下で頭蓋骨に小さな孔(こう)を開け、ガイドに沿って細い針を脳深部の被殻まで進め、左右両側の被殻に複数箇所へ分けて細胞を移植する定位脳手術です。点滴で投与する薬ではなく、専用の手術設備と神経外科チームを備えた限られた施設でのみ実施可能です。
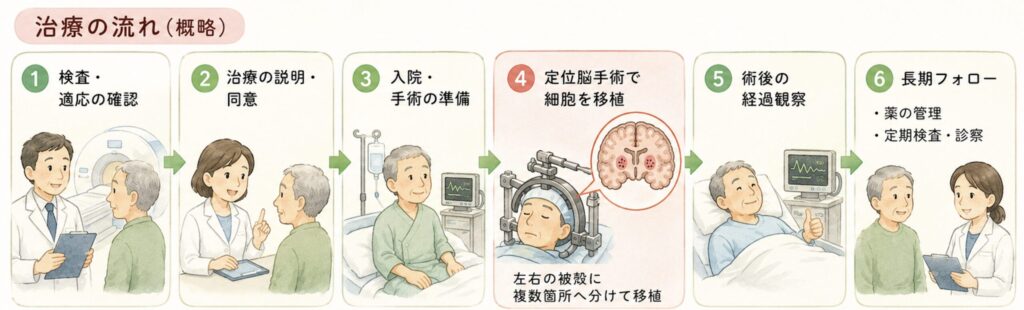
治療の流れ(概略)
- 適応評価:神経内科・脳神経外科による精密検査、MRI、レボドパ反応性評価
- 治療同意・施設要件確認:条件・期限付承認下のため、最適使用推進ガイドライン対象施設での実施
- 入院:手術前検査、麻酔評価
- 定位脳手術:全身麻酔下で頭蓋骨に小孔を作成→定位フレームによるガイド下に、ドパミン神経前駆細胞を左右両側の被殻に複数箇所、分割移植
- 術後管理:入院での経過観察(出血・感染・移植細胞の異常増殖モニタリング)
- 長期フォロー:免疫抑制薬の投与期間管理、定期的なMRI・PET・運動症状評価
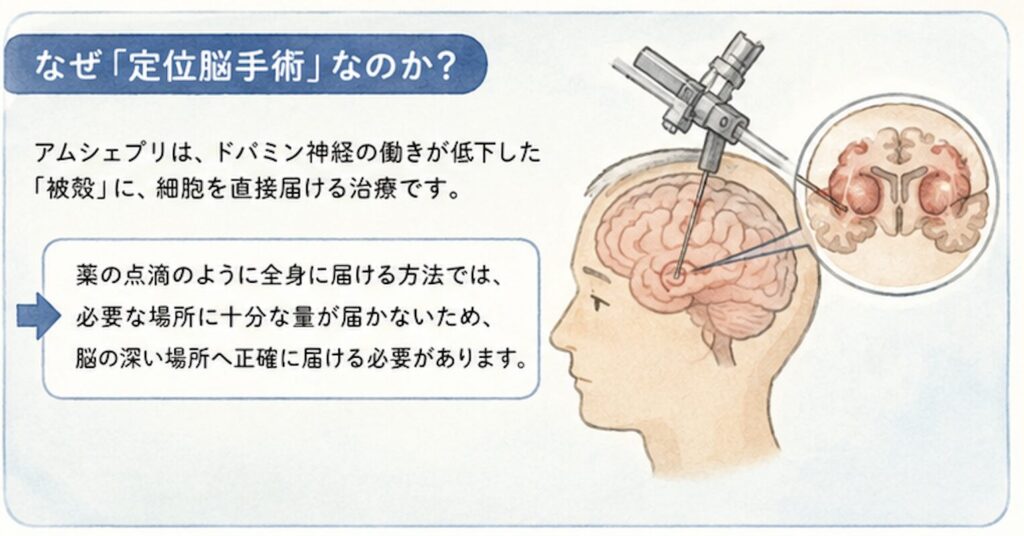
投与経路としての「定位脳手術」が意味すること
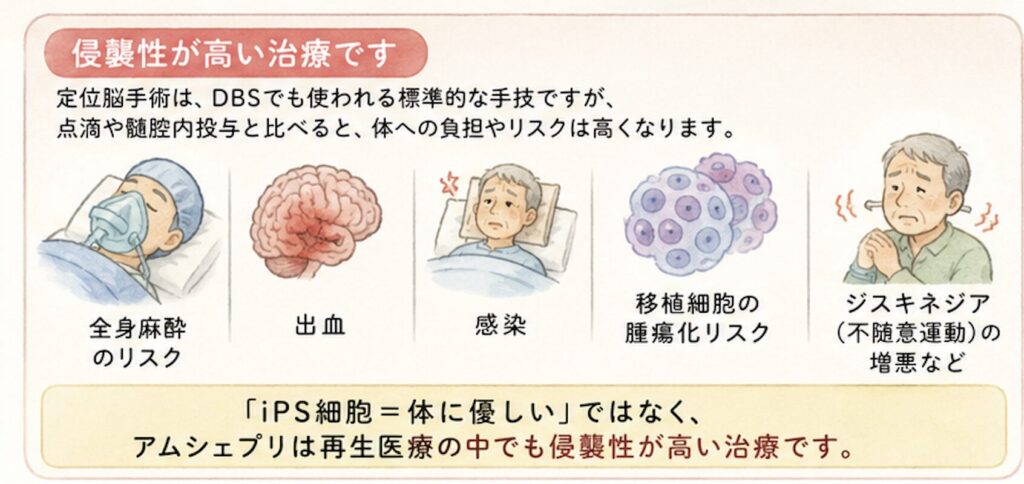
定位脳手術は、脳深部刺激療法(DBS)でも使われている脳神経外科の標準的な手技ですが、点滴投与や髄腔内投与と比べると侵襲性は明らかに高い処置です。全身麻酔リスク、出血、感染、移植細胞の腫瘍化リスク、ジスキネジアの増悪などはゼロにはできません。
「iPS細胞=最先端=体に優しい」というイメージとは異なり、アムシェプリは再生医療の中でも投与経路の侵襲性が高い部類に入る、という理解は重要です。
薬価5,530万円とパーキンソン病における保険適用——患者負担はどうなるか
▼ ダイレクトアンサー 中央社会保険医療協議会(中医協)は2026年5月13日にアムシェプリの薬価を1患者あたり5,530万6,737円と決定し、5月20日から保険適用が開始されました。iPS細胞由来製品の保険適用は世界初です。患者個人の窓口負担は高額療養費制度により大幅に軽減されます。
薬価と費用構造
| 項目 | 内容 |
|---|---|
| 薬価(1患者あたり) | 5,530万6,737円 |
| 適用開始日 | 2026年5月20日 |
| 保険適用 | あり(中医協 2026年5月13日了承) |
| 承認形態 | 条件及び期限付承認(期限:最長7年) |
| 製造販売 | 住友ファーマ株式会社 |
| 適応 | レボドパを含む既存治療で十分な効果が得られないパーキンソン病患者さんの運動症状改善 |
薬価は薬剤費のみで、これに入院費・定位脳手術費・術前後の検査費・免疫抑制薬費などが別途加算されます。ただし高額療養費制度の対象となるため、所得区分に応じて患者個人の自己負担は月数万円〜数十万円程度に収まる設計です。
iPS細胞 × 保険適用が意味すること
iPS細胞は2006年に山中伸弥教授らが樹立してから20年。その間、再生医療の臨床応用は研究段階で停滞しがちでした。今回の保険適用は「iPS細胞研究が、ようやく日本の医療制度に乗った」歴史的な転換点であり、今後、心臓再生(リハート)、網膜、軟骨など他疾患領域への波及が期待されます。
一方で、5,530万円という薬価は社会全体で支える医療費の話でもあり、再生医療が他疾患に広がる際の薬価設定の持続可能性は、今後の社会的議論になっていく見込みです。
京大Phase I/II試験のエビデンス——パーキンソン病iPS細胞治療で何が示されたか
▼ ダイレクトアンサー アムシェプリの承認根拠となった京都大学のPhase I/II試験では、50〜69歳のパーキンソン病患者7名にiPS細胞由来ドパミン神経前駆細胞を両側被殻に移植し、約2年間観察した結果、重篤な有害事象は発生せず、有効性評価対象6名のうち4名でオフ時のMDS-UPDRS Part IIIスコアが改善し、PETでもドパミン神経活動の増加が示されました(Nature, 2025)。
試験デザインのポイント
- 対象:50〜69歳のパーキンソン病患者 7名
- 投与法:iPS細胞由来ドパミン神経前駆細胞を両側被殻に移植
- 観察期間:約2年
- 評価指標:MDS-UPDRS Part III(運動症状スコア)、安全性、画像所見(MRI/PET)
主な結果
| 項目 | 結果 |
|---|---|
| 重篤な有害事象 | 観察されず |
| MRI上の移植組織異常増殖 | 認められず |
| MDS-UPDRS Part III改善 | 評価対象6名中4名で改善 |
| PETでのドパミン神経活動 | 増加が示された |
| 出典 | Nature 2025(京都大学CiRA) |
この試験の意味と限界
「7名・2年観察」というサンプル規模は、率直に言えばまだ小さい。けれども第I/II相試験としては安全性プロファイルが確認され、有効性のシグナルが見えた——これは細胞移植治療における極めて重要な一歩です。
ただし、これらの結果がそのまま「一般のパーキンソン病患者さんに常に効く」ことを意味するわけではありません。条件・期限付承認下で進められる第Ⅳ相試験(製造販売後臨床試験)で症例数が積み上がってはじめて、効果の大きさ・持続期間・副作用プロファイルの全体像が見えてきます。
もう一つの選択肢——自家脂肪由来幹細胞(ADSC)治療
▼ ダイレクトアンサー 自家脂肪由来幹細胞(ADSC)治療は、自分自身の脂肪から採取した間葉系幹細胞を培養し、静脈点滴や髄腔内投与などの低侵襲ルートで投与する再生医療です。アムシェプリのような開頭手術を伴わず、神経炎症の調整や栄養因子の供給を狙うアプローチで、パーキンソン病に対しても自費診療として日本国内で実施可能です。
自家脂肪由来幹細胞治療の基本コンセプト
自家脂肪由来幹細胞は、腹部などから少量の脂肪を局所麻酔下で採取し、専用の細胞培養施設で増殖させた後、患者さん本人に戻す治療です。投与経路は静脈内点滴が中心で、髄腔内投与(腰椎穿刺)が併用される場合もあります。
自家脂肪由来幹細胞の主な作用機序は以下の通りです。
- 神経保護作用:BDNF・GDNFなどの神経栄養因子を分泌し、残存神経の生存をサポート
- 抗炎症作用:脳内の慢性炎症を抑制するサイトカインを分泌
- 血管新生・組織修復促進:VEGFなどの成長因子放出
- 免疫調整作用:間葉系幹細胞特有の免疫モジュレーション
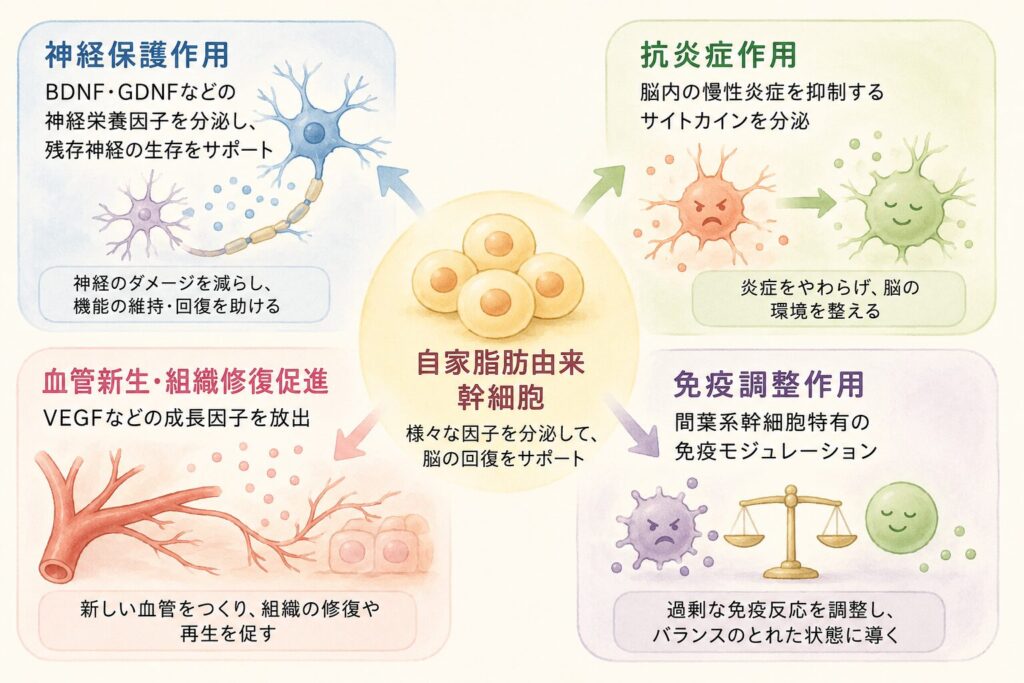
自家脂肪由来幹細胞がパーキンソン病で期待される理由
国内外の症例報告や小規模試験で、自家ADSCを複数回点滴投与した患者さんの一部で、MDS-UPDRSスコアやPDQ-39(QOL指標)の改善が報告されており、現時点で重篤な副作用は限定的とされています。プラセボ対照の大規模試験はまだ進行中で、エビデンスレベルとしては「研究段階」に位置づけられます。
なお、自家脂肪由来幹細胞治療の作用メカニズム・症例報告・投与法の詳細については、Cell Grand Clinicの別コラムで詳しく解説しています。
アムシェプリ vs 自家脂肪由来幹細胞(ADSC)治療——どう選ぶか
▼ ダイレクトアンサー アムシェプリ(他家iPS由来)と自家脂肪由来幹細胞(ADSC)治療は、同じ「再生医療」でも投与経路・侵襲性・コスト・適応範囲が大きく異なります。アムシェプリは保険診療で根本的な細胞補充を狙う一方、開頭手術が必要です。自家脂肪由来幹細胞は自費診療ですが、低侵襲で神経保護・抗炎症を狙うアプローチです。
比較表
| 項目 | アムシェプリ(他家iPS由来) | 自家脂肪由来幹細胞 |
|---|---|---|
| 細胞のもと | 他人のiPS細胞由来ドパミン神経前駆細胞 | 自分の脂肪由来間葉系幹細胞 |
| 投与経路 | 定位脳手術で脳内(被殻)に移植 | 主に静脈点滴・髄腔内投与 |
| 侵襲性 | 高(開頭・全身麻酔・入院) | 比較的低(脂肪採取+点滴) |
| 拒絶反応 | 免疫抑制が必要 | 原則不要(自家細胞) |
| 治療コンセプト | 神経細胞の補充・再生 | 神経保護・抗炎症・栄養因子供給 |
| 保険適用 | あり(2026年5月20日〜) | なし(自費診療) |
| 患者負担 | 高額療養費制度で月数万〜数十万円 | 自費(自己負担) |
| 承認形態 | 条件・期限付承認(期限7年) | 厚労省再生医療等提供計画に基づく自由診療 |
| 適応の確かさ | 「レボドパ効果不十分」が中心 | 適応・症例選択は施設の責任で判断 |
| エビデンス | 京大Phase I/II(n=7、Nature 2025) | 症例報告・小規模試験が蓄積中 |
患者さんが選択するときの考え方
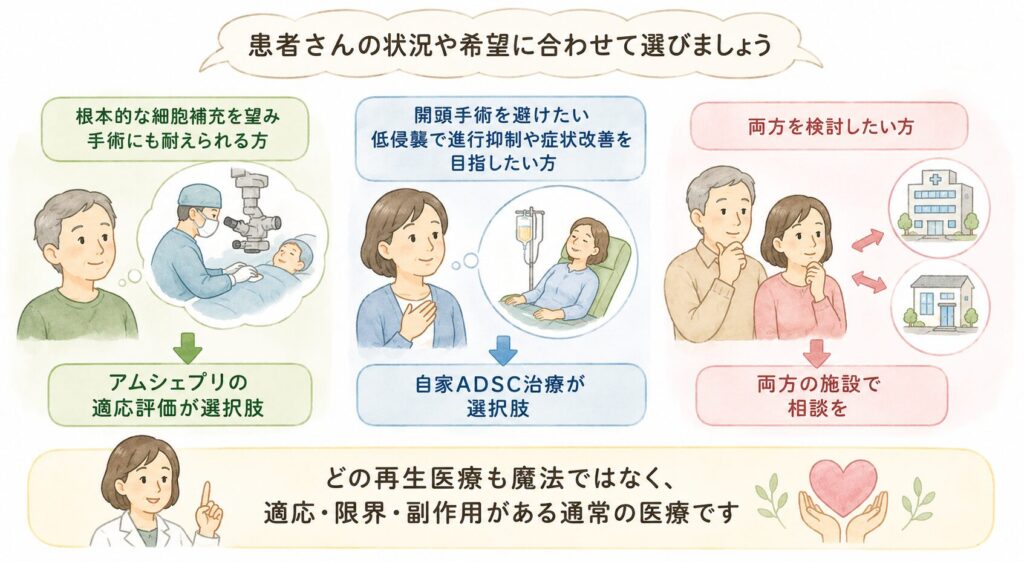
どちらが優れている、という単純な話ではありません。患者さんの病状・進行度・全身状態・希望(侵襲性をどこまで受け入れるか)・通院可能性・費用面で、適した選択は変わります。
- 進行期で薬が効きにくく、根本的な細胞補充を望み、手術にも耐えられる方 → アムシェプリの適応評価が選択肢
- 開頭手術を避けたい、進行抑制と症状改善を低侵襲で狙いたい方 → 自家ADSC治療が選択肢
- 両方を検討したい方 → アムシェプリ施設と再生医療クリニックの両方で相談を
「どの再生医療も魔法ではなく、適応・限界・副作用がある通常の医療」——これは強調しておくべき点です。
パーキンソン病でお悩みの方へ——Cell Grand Clinicができるサポート
▼ ダイレクトアンサー Cell Grand Clinicは大阪・心斎橋の再生医療クリニックで、厚生労働省に再生医療等提供計画13件を届出済み(大阪最多水準)、米国再生医療学会専門医(ABRM)による自家脂肪由来幹細胞治療を3,000症例超実施しています。パーキンソン病そのものを直接適応とした自家ADSC治療は厚労省提供計画外のため当院では実施しておりませんが、患者さんの全身状態を整え、薬物療法やリハビリの効果を最大化するためのエクソソーム治療・フレイル枠での全身再生医療・動脈硬化治療・NMN点滴などをご提供しています。
Cell Grand Clinicが「現実的に」できること
パーキンソン病そのものを根治させる治療は、現時点では世界中どの施設にもありません。Cell Grand Clinicが大切にしているのは、「患者さんの全身状態と生活の質を整えることで進行を緩やかにし、薬物治療やリハビリの効果を最大化する」というアプローチです。
① エクソソーム治療——もっとも始めやすい再生医療の入口
幹細胞が分泌する有効成分(成長因子・サイトカイン・miRNA)を抽出した製剤を、点滴または点鼻で投与する治療です。脂肪採取が不要で、1回30分の点滴から始められます。神経炎症の抑制・脳血流改善・抗酸化作用が期待され、認知機能の維持を目的とした研究も進んでいます。「いきなり幹細胞治療はハードルが高い」という方に最初の選択肢として最も多く選ばれています。
② フレイル枠での全身再生医療(厚労省第二種再生医療等提供計画 PB5250049)
パーキンソン病の進行に伴い、筋力低下・体重減少・歩行能力低下といったフレイル(虚弱)状態が併発しやすくなります。Cell Grand Clinicはフレイルに対する第二種再生医療等提供計画を届出済みで、この枠組みで自家脂肪由来幹細胞による全身アンチエイジング・未病対策治療をご提供できます。神経炎症の抑制、ミトコンドリア機能の改善、筋肉量・体力の維持を狙う「全身を整える」アプローチです。
③ 動脈硬化治療(厚労省第二種再生医療等提供計画 PB5250051)
パーキンソン病の方は、脳血流の低下や血管年齢の上昇を併発する例が少なくありません。動脈硬化に対する自家脂肪由来幹細胞治療を厚労省届出枠で実施しており、結果として血管系の若返り・脳血流のサポートも期待されます。
④ NMN点滴・PRP——補完的な選択肢
NAD+前駆体であるNMNの点滴は、ミトコンドリア機能のサポート・全身の代謝改善を狙う選択肢。PRP(多血小板血漿)も成長因子による組織修復を目的に併用可能です。
Cell Grand Clinicが選ばれる「6つの理由」
| # | 理由 | 患者さんから見た意味 |
|---|---|---|
| 1 | 3,000症例超の臨床実績 | 米国再生医療学会専門医(ABRM)認定の院長が、これまで約20カ国の患者さんに対し3,000件を超える幹細胞治療を実施 |
| 2 | 厚労省届出13件=大阪最多水準 | 第二種10件+第三種3件を届出済み(Alzheimer病は2026年7月運用開始予定で14件目)。各疾患に対し法的根拠を備えた治療をご提供 |
| 3 | 「本物の幹細胞か」を世界基準で検査 | 国際細胞治療学会(ISCT)が定めた世界共通のルールで、一つひとつ「これは確かに間葉系幹細胞である」と確認できた細胞だけを使用。基準を満たさない細胞は廃棄 |
| 4 | 「生きている細胞」を95%以上保証 | 死んだ細胞では治療効果は出ません。投与直前まで品質を確認し、生存率95%以上を満たした細胞だけを体に戻します |
| 5 | 「若い細胞」だけを使う | 細胞は培養を重ねるほど老化し、再生力が低下します。Cell Grand Clinicは若い段階(Passage 3で培養停止)の細胞のみを使用 |
| 6 | 院長が最初から最後まで一貫担当 | 問い合わせ→評価→採取→培養→投与→1ヶ月・3ヶ月・6ヶ月フォローまで、医師が引き継ぎなく責任を持って対応 |
患者さんの「期待値」を一緒に整理する
新しい治療(アムシェプリのような)の登場を素直に評価しつつ、足元の臨床——エクソソーム・フレイル枠・動脈硬化治療といった既存の再生医療——も丁寧に育てていく。それがCell Grand Clinicの基本姿勢です。患者さんに「冷静な期待値」を持っていただくことを最優先に、根拠と説明を尽くしたうえでの治療選択を支援します。
FAQ——よくある質問
▼ ダイレクトアンサー アムシェプリ・パーキンソン病iPS細胞治療・自家ADSC治療について、患者さんからよく寄せられる質問にお答えします。
Q1. アムシェプリはいつから受けられますか?
A. 2026年5月20日から保険適用が開始されています。ただし、最適使用推進ガイドラインの対象製品で、専用の体制を備えた施設でのみ実施可能なため、医療機関・地域によって実施開始時期は異なります。担当医にご相談ください。
Q2. アムシェプリの薬価はいくらですか?患者の自己負担は?
A. 薬剤費の薬価は1患者あたり5,530万6,737円です。これに入院費・手術費が加わりますが、高額療養費制度の対象となるため、所得区分に応じて月数万円〜数十万円程度に自己負担が抑えられる設計です。
Q3. 「条件・期限付承認」とは何ですか?
A. 限られたデータで有効性が推定され、安全性が確認された段階で、条件を付して早期に患者さんに届け、その後に追加データを集めて本承認を目指す制度です。アムシェプリの期限は最長7年で、この期間中に第Ⅳ相試験のデータが蓄積されます。
Q4. 誰でもアムシェプリを受けられますか?
A. いいえ。レボドパを含む既存治療で十分な効果が得られないパーキンソン病患者さんが対象で、全身麻酔下の定位脳手術に耐えられる全身状態、長期通院の可能性、施設の受け入れ体制など複数の条件があります。
Q5. アムシェプリと自家脂肪由来幹細胞治療はどう違いますか?
A. アムシェプリは他人のiPS細胞由来の細胞を定位脳手術で被殻に移植する保険診療。自家脂肪由来幹細胞(ADSC)治療は自分の脂肪から採取した細胞を点滴で投与する自費診療です。投与経路・侵襲性・適応の考え方が大きく異なります。
Q6. パーキンソン病に対する自家幹細胞治療は保険が効きますか?
A. いいえ。自家脂肪由来幹細胞(ADSC)によるパーキンソン病治療は現時点では自費診療です。厚生労働省への再生医療等提供計画届出に基づき、認定再生医療クリニックで実施されています。
Q7. 開頭手術を避けたい場合の選択肢はありますか?
A. はい。低侵襲な選択肢として、自家脂肪由来幹細胞(ADSC)の点滴投与による治療があります。神経保護・抗炎症・栄養因子供給を狙うアプローチで、症例報告と小規模試験のデータが蓄積されつつあります。
Q8. アムシェプリの副作用にはどのようなものがありますか?
A. 全身麻酔リスク、術後の出血・感染、移植細胞の異常増殖、ジスキネジアの増悪などが想定されます。条件・期限付承認下で進められる第Ⅳ相試験で、より詳細な副作用プロファイルが今後明らかになります。
{ “@context”: “https://schema.org”, “@type”: “FAQPage”, “mainEntity”: [ { “@type”: “Question”, “name”: “アムシェプリはいつから受けられますか?”, “acceptedAnswer”: { “@type”: “Answer”, “text”: “2026年5月20日から保険適用が開始されています。ただし、最適使用推進ガイドラインの対象製品で、専用の体制を備えた施設でのみ実施可能なため、医療機関・地域によって実施開始時期は異なります。” } }, { “@type”: “Question”, “name”: “アムシェプリの薬価はいくらですか?患者の自己負担は?”, “acceptedAnswer”: { “@type”: “Answer”, “text”: “薬剤費の薬価は1患者あたり5,530万6,737円です。高額療養費制度の対象となるため、所得区分に応じて月数万円〜数十万円程度に自己負担が抑えられる設計です。” } }, { “@type”: “Question”, “name”: “条件・期限付承認とは何ですか?”, “acceptedAnswer”: { “@type”: “Answer”, “text”: “限られたデータで有効性が推定され、安全性が確認された段階で条件を付して早期に届け、その後に追加データを集めて本承認を目指す制度です。アムシェプリの期限は最長7年です。” } }, { “@type”: “Question”, “name”: “誰でもアムシェプリを受けられますか?”, “acceptedAnswer”: { “@type”: “Answer”, “text”: “いいえ。レボドパを含む既存治療で十分な効果が得られないパーキンソン病患者さんが対象で、全身麻酔下の定位脳手術に耐えられる全身状態、施設の受け入れ体制など複数の条件があります。” } }, { “@type”: “Question”, “name”: “アムシェプリと自家脂肪由来幹細胞治療はどう違いますか?”, “acceptedAnswer”: { “@type”: “Answer”, “text”: “アムシェプリは他人のiPS細胞由来の細胞を定位脳手術で被殻に移植する保険診療。自家脂肪由来幹細胞治療は自分の脂肪から採取した細胞を点滴で投与する自費診療で、投与経路・侵襲性・適応の考え方が大きく異なります。” } }, { “@type”: “Question”, “name”: “パーキンソン病に対する自家幹細胞治療は保険が効きますか?”, “acceptedAnswer”: { “@type”: “Answer”, “text”: “いいえ。自家脂肪由来幹細胞によるパーキンソン病治療は現時点では自費診療です。厚生労働省への再生医療等提供計画届出に基づき、認定再生医療クリニックで実施されています。” } }, { “@type”: “Question”, “name”: “開頭手術を避けたい場合の選択肢はありますか?”, “acceptedAnswer”: { “@type”: “Answer”, “text”: “はい。低侵襲な選択肢として、自家脂肪由来幹細胞(ADSC)の点滴投与による治療があります。神経保護・抗炎症・栄養因子供給を狙うアプローチで、症例報告と小規模試験のデータが蓄積されつつあります。” } }, { “@type”: “Question”, “name”: “アムシェプリの副作用にはどのようなものがありますか?”, “acceptedAnswer”: { “@type”: “Answer”, “text”: “全身麻酔リスク、術後の出血・感染、移植細胞の異常増殖、ジスキネジアの増悪などが想定されます。第Ⅳ相試験で詳細な副作用プロファイルが今後明らかになります。” } } ] }まとめ——希望と現実、両方を持って前に進む
▼ ダイレクトアンサー アムシェプリの保険適用は、iPS細胞研究20年の積み上げが日本の医療制度に乗った歴史的瞬間です。一方で投与は開頭手術を伴い、効果と副作用の全体像はこれからの第Ⅳ相試験で明らかになっていきます。「どの再生医療も魔法ではない」という冷静な視点と、自家ADSC治療など別ルートの選択肢を含めた総合的な判断が大切です。
- アムシェプリは世界初のiPS細胞由来再生医療等製品として保険適用へ(薬価5,530万円、2026年5月20日〜)
- 投与は定位脳手術+被殻移植で、再生医療の中でも侵襲性は高い部類
- 京大Phase I/II試験で安全性と有効性のシグナルは示されたが、エビデンスは7年の第Ⅳ相試験で本格的に積み上がる段階
- 自家脂肪由来幹細胞(ADSC)治療は、低侵襲・自費診療の選択肢として並走している
- どの治療も「魔法」ではない。正しい期待値設定が患者さんを守る最大の力
パーキンソン病で苦しむご本人・ご家族にとって、選択肢が増えること自体が大きな救いです。新しい治療を喜びつつ、足元の臨床も丁寧に育てる——その両輪が、再生医療を本当に社会に根付かせる道です。
関連コラム
- パーキンソン病への最新治療「幹細胞治療」(自家ADSCの作用機序・投与法・症例の詳細解説)
- 【2026年最新】多発性硬化症(MS)に対する脂肪由来幹細胞治療
- 多系統萎縮症(MSA)の最新治療|2026年版・医師がエビデンスで総まとめ
- 脳梗塞の後遺症は治る?症状・回復過程・最新治療を医師が解説
- 神経障害に挑む幹細胞治療【再生医療の最前線】
- 再生医療のメリット・デメリット〜専門医が語る治療選択の判断基準
引用文献
- Sawamoto N, Takahashi J, et al. Phase I/II trial of iPS-cell-derived dopaminergic cells for Parkinson’s disease. Nature. 2025. doi:10.1038/s41586-025-08700-0
- 住友ファーマ株式会社. アムシェプリ製品情報・適正使用ガイド. 2026年5月更新. https://sumitomo-pharma.jp/product/amchepry/
- 中央社会保険医療協議会 総会資料(2026年5月13日). 厚生労働省.
- Li K, Li X, Shi G, et al. Effectiveness and mechanisms of adipose-derived stem cell therapy in animal models of Parkinson’s disease: a systematic review and meta-analysis. Translational Neurodegeneration. 2021;10(1):14.
- Wang F, Sun Z, Peng D, et al. Cell-therapy for Parkinson’s disease: a systematic review and meta-analysis. Journal of Translational Medicine. 2023;21(1):601.
- Schiess M, Suescun J, Doursout MF, et al. Allogeneic bone marrow–derived mesenchymal stem cell safety in idiopathic Parkinson’s disease. Movement Disorders. 2021;36(8):1825-1834.
- Vij R, Kim H, Park H, et al. Safety and efficacy of adipose-derived mesenchymal stem cell therapy in elderly Parkinson’s disease patients: an intermediate-size expanded access program. Cytotherapy. 2025;27(2):181-187.
- International Parkinson and Movement Disorder Society (MDS) Scientific Issues Committee. MDS Position Paper – Use of Stem Cell Therapies for Parkinson’s Disease. January 2021.
最終更新日:2026.05.15





とは?老化を招く体内の焦げつき-150x84.png)






